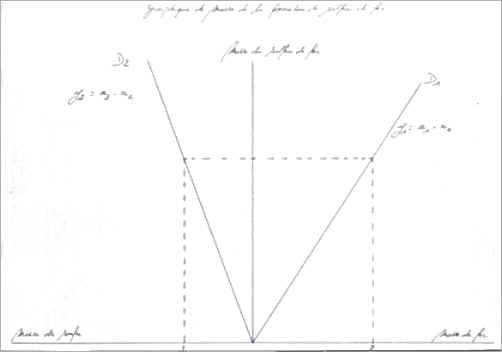
Le graphique des masses d'une réaction d'association se présente sous la forme classique en mathématique d'un graphique orthonormé. L'axe des Y (ordonnées) est occupé par la masse du corps pur formé lors de la réaction. L'axe des X (abscisses) est occupé à droite de l'origine des axes (0,0) par la masse de l'un des deux réactifs, à gauche de l'origine des axes (0,0) par la masse de l'autre réactif.
Envisageons tout d'abord la réaction d'association du fer et du soufre pour former du sulfure de fer. Le premier point du graphique est facilement connu: 0 gramme de soufre réagit avec 0 gramme de fer pour former 0 gramme de sulfure de fer. Les données suivantes nous serviront à placer les deux points suivants: 7 grammes de fer réagissent avec 4 grammes de soufre pour former 11 grammes de sulfure de fer. Traçons notre graphique sur du papier millimétré. Nous obtenons deux demi-droites passant par l'origine. L'équation mathématique d'une droite passant par l'origine des axes est notée Y = a X où a est appelé la pente de la droite. La valeur numérique de la pente peut être calculée: il s'agit du quotient Y/X.
Dans notre cas ce quotient représente le calcul du rapport des masses du corps pur formé et d'un réactif. Nous avons deux demi-droites et donc deux pentes différentes: une pour chaque réactif.

Comment pouvons-nous déterminer la valeur du rapport des masses des réactifs?
Soit la demi-droite D1 d'équation: Y1 = a1 X1
Soit la demi-droite D2 d'équation: Y2 = a2 X2
Nous avons:
a1 = Y1/X1 = Masse du sulfure de fer / Masse du soufre = 2.75
a2 = Y2/X2 = Masse du sulfure de fer / Masse du fer = 1.57
et donc: a1/a2 = (masse du sulfure de fer / masse du soufre) /
(masse du sulfure de fer/masse du fer) =
masse du fer / masse du soufre = 1.75
Toute réaction d'association peut être traduite sous la forme d'un graphique des masses. La pente d'une droite nous donne la valeur du rapport des masses du produit formé et d'un réactif. La valeur du rapport des deux pentes nous donne la valeur du rapport des masses des réactifs. Ces quotients sont constants pour une combinaison donnée et propre à chaque combinaison.
il est

|

|
|
Vous pouvez envoyer vos commentaires et suggestions:
pierre_hebrant@yahoo.fr |
Vous pouvez aussi m'écrire: Hebrant pierre Athénée Royal Bruxelles 2 - Rue de Molenbeek, 72-74 à 1020 Bruxelles.
|